复分解反应,是四大基本反应类型之一。复分解反应是由 两种 化合物 互相交换成分,生成 另外两种化合物的反应。复分解反应的实质是发生复分解反应的两种物质在水溶液中交换离子,结合成难电离的物质—— 沉淀 、气体或弱电解质(最常见的为水)。可简记为 AB+CD→AD+CB。

1基本介绍
复分解反应是化学中 四大基本 反应类型 之一。要理解它必须抓住概念中的“化合物”和“互相交换成分”这两个关键词。酸、 碱、 盐溶液间发生的反应一般是两种化合物相互交换成分而形成的,即参加复分解反应的化合物在 水溶液中发生 电离并解离成自由移动的离子,离子间重新组合成新的化合物。因此酸、碱、盐溶液间的反应一般是复分解反应。
2发生条件
基本条件:发生复分解反应的两种物质能在水溶液中交换离子,结合成难电离的物质( 沉淀 、气体或弱电解质)。

1、 碱性氧化物+酸:酸的酸性较强(如HCl、H2SO4、HNO3等),可发生反应。
2、酸+碱( 中和反应):当酸、碱都很弱时,不发生反应。
3、酸+盐:强酸制 弱酸;交换离子后有沉淀;强酸与碳酸盐反应;满足一个条件即可发生反应。
4、碱+盐:强碱与 铵盐反应;两种反应物都可溶、交换离子后有沉淀、水、气体三者之一;满足一个条件即可发生反应。
5、盐+盐:两种反应物都可溶,交换离子后有沉淀、水、气体三者之一,满足一个条件即可发生反应。
3相关示例
氢氧化钠 氯化钡 硫酸铜之间的反应
碳酸钠和氢氧化钙的反应
探究溶液中复分解反应的条件
方程式记忆指导
概括上述五种类型的复分解反应能够发生并趋于完成的条件,可分成两方面记忆掌握。一方面是对反应物的要求:酸盐、酸碱一般行,盐盐、盐碱都需溶;另一方面是对生成物的要求:生成物中有沉淀析出或有气体放出,或有水等弱电解质生成。这两方面必须兼顾,才能正确地书写有关复分解反应的化学方程式。
4特别注意
注意点一:
特别要注意的是,碱+非金属氧化物→盐+水的反应不是复分解反应。
因为根据复分解反应的定义。只有两种化合物互相交换成分,生成两种新的化合物的反应才是复分解反应。
注意点二:
酸+ 金属氧化物→盐+水,属于复分解反应。
碱+ 非金属氧化物→盐+水,不属于复分解反应。
5复分解反应总结
复分解反应是两种化合物互相交换成分生成另外两种化合物的反应。其实质是两种化合物在溶液中发生离子互换,即同时互换阳离子或同时互换阴离子。可简记为AB+CD=AD+CB。
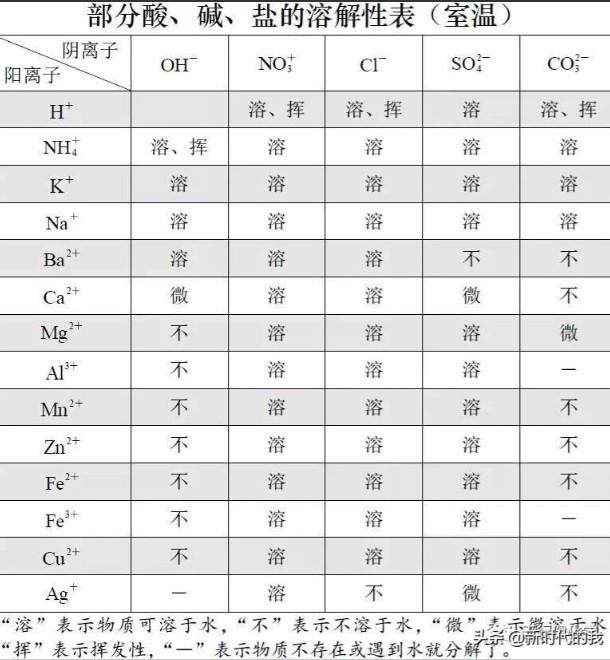
复分解反应的本质是溶液中的离子结合成难电离的物质(如水)、难溶的物质(如沉淀)或挥发性气体,而使复分解反应趋于完成。为了准确判别复分解反应的发生,必须熟记常见酸、碱、盐的溶解性表,正确地运用物质的溶解性。
欢迎关注微信公众号:中学高分宝典

 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏